![]()

Глава 5. Свойства
Белки имеют высокую молекулярную массу, некоторые растворимы в воде, способны к набуханию, характеризуются оптической активностью, подвижностью в электрическом поле и некоторыми другими свойствами.
Белки активно вступают в химические реакции. Это свойство связано с тем, что аминокислоты, входящие в состав белков, содержат разные функциональные группы, способные реагировать с другими веществами. Важно, что такие взаимодействия происходят и внутри белковой молекулы, в результате чего образуется пептидная, водородная дисульфидная и другие виды связей. К радикалам аминокислот, а следовательно и белков, могут присоединяться различные соединения и ионы, что обеспечивает их транспорт по крови.
Белки
являются высокомолекулярными соединениями. Это полимеры,
состоящие из сотен и тысяч аминокислотных остатков
- мономеров. Соответственно и молекулярная масса
белков находится в пределах 10 000 - 1 000 000.
Так, в составе рибонуклеазы (фермента, расщепляющего
РНК) содержится 124 аминокислотных остатка и ее
молекулярная масса составляет примерно 14 000. Миоглобин
(белок мышц), состоящий из 153 аминокислотных остатков,
имеет молекулярную массу 17 000, а гемоглобин -
64 500 (574 аминокислотных остатка). Молекулярные
массы других белков более высокие: ![]() -глобулин
(образует антитела) состоит из 1250 аминокислот
и имеет молекулярную массу около 150 000, а молекулярная
масса фермента глутаматдегидрогеназы превышает 1
000 000.
-глобулин
(образует антитела) состоит из 1250 аминокислот
и имеет молекулярную массу около 150 000, а молекулярная
масса фермента глутаматдегидрогеназы превышает 1
000 000.
Определение молекулярной массы проводится различными методами: осмометрическим, гельфильтрационным, оптическим и др. однако наиболее точным является метод седиментации, предложенный Т. Сведбергом. Он основан на том, что при ультрацентрифугировании ускорением до 900 000 g скорость осаждения белков зависит от их молекулярной массы.
Важнейшим свойством белков является их способность проявлять как кислые так и основные, то есть выступать в роли амфотерных электролитов. Это обеспечивается за счет различных диссоциирующих группировок, входящих в состав радикалов аминокислот. Например, кислотные свойства белку придают карбоксильные группы аспарагиновой глутаминовой аминокислот, а щелочные - радикалы аргинина, лизина и гистидина. Чем больше дикарбоновых аминокислот содержится в белке, тем сильнее проявляются его кислотные свойства и наоборот.
Эти же группировки имеют и электрические заряды, формирующие общий заряд белковой молекулы. В белках, где преобладают аспарагиновая и глутаминовая аминокислоты, заряд белка будет отрицательным, избыток основных аминокислот придает положительный заряд белковой молекуле. Вследствие этого в электрическом поле белки будут передвигаться к катоду или аноду в зависимости от величины их общего заряда. Так, в щелочной среде (рН 7 - 14) белок отдает протон и заряжается отрицательно, тогда как в кислой среде (рН 1 - 7) подавляется диссоциация кислотных групп и белок становится катионом.
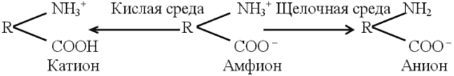
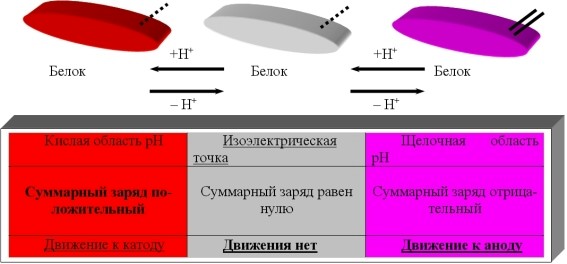
Таким образом, фактором, определяющим поведение белка как катиона или аниона, является реакция среды, которая определяется концентрацией водородных ионов и выражается величиной рН. Однако при определенных значениях рН число положительных и отрицательных зарядов уравнивается и молекула становится электронейтральной, т.е. она не будет перемещаться в электрическом поле. Такое значение рН среды определяется как изоэлектрическая точка белков. При этом белок находится в наименее устойчивом состоянии и при незначительных изменениях рН в кислую или щелочную сторону легко выпадает в осадок. Для большинства природных белков изоэлектрическая точка находится в слабокислой среде (рН 4,8 - 5,4), что свидетельствует о преобладании в их составе дикарбоновых аминокислот.
Свойство
амфотерности лежит в основе буферных свойств белков
и их участии в регуляции рН крови. Величина рН крови
человека отличается постоянством и находится в пределах
7,36 - 7,4 , несмотря на различные вещества кислого
или основного характера, регулярно поступающие с
пищей или образующиеся в обменных процессах - следовательно
существуют специальные механизмы регуляции кислотно-щелочного
равновесия внутренней среды организма. К таким системам
относится гемоглобиновая буферная система. Изменение
рН крови более чем на 0,07 свидетельствует о развитии
патологического процесса. Сдвиг рН в кислую сторону
называется ацидозом, а в щелочную - алкалозом.
Важное значение для организма имеет способность
белков адсорбировать на своей поверхности некоторые
вещества и ионы (гормоны, витамины, железо, медь),
которые либо плохо растворимы в воде, либо являются
токсичными (билирубин, свободные жирные кислоты).
Белки транспортируют их по крови к местам дальнейших
превращений или обезвреживания.
Водные растворы белков имеют свои особенности. Во-первых, белки обладают большим сродством к воде, т.е. они гидрофильны. Это значит, что молекулы белка, как заряженные частицы, притягивают к себе диполи воды, которые располагаются вокруг белковой молекулы и образуют водную или гидратную оболочку. Эта оболочка предохраняет молекулы белка от склеивания и выпадения в осадок. Величина гидратной оболочки зависит от структуры белка. Например, альбумины более легко связываются с молекулами воды и имеют относительно большую водную оболочку, тогда как глобулины, фибриноген присоединяют воду хуже, и гидратная оболочка и них меньше. Таким образом, устойчивость водного раствора белка определяется двумя факторами: наличием заряда белковой молекулы и находящейся вокруг нее водной оболочки. При удалении этих факторов белок выпадает в осадок. Данный процесс может быть обратимым и необратимым.
Обратимое осаждение белков (высаливание) предполагает выпадение белка в осадок под действием определенных веществ, после удаления которых он вновь возвращается в свое исходное (нативное) состояние. Для высаливания белков используют соли щелочных и щелочноземельных металлов (наиболее часто в практике используют сульфат натрия и аммония). Эти соли удаляют водную оболочку (вызывают обезвоживание) и снимают заряд. Между величиной водной оболочки белковых молекул и концентрацией солей существует прямая зависимость: чем меньше гидратная оболочка, тем меньше требуется солей. Так, глобулины, имеющие крупные и тяжелые молекулы и небольшую водную оболочку, выпадают в осадок при неполном насыщении раствора солями, а альбумины как более мелкие молекулы, окруженные большой водной оболочкой, - при полном насыщении.
Необратимое осаждение связано с глубокими внутримолекулярными изменениями структуры белка, что приводит в потере ими нативных свойств (растворимости, биологической активности и др.). Такой белок называется денатурированным, а процесс денатурацией. Денатурация белков происходит в желудке, где имеется сильнокислая среда (рН 0,5 - 1,5), и это способствует расщеплению белков протеолитическими ферментами. Денатурация белков положена в основу лечения отравления тяжелыми металлами, когда больному вводят per os ("через рот") молоко или сырые яйца с тем, чтобы металлы денатурируя белки молока или яиц. Адсорбировались на их поверхности и не действовали на белки слизистой оболочки желудка и кишечника, а также не всасывались в кровь.


Размер белковых молекул лежит в пределах 1 мкм до 1 нм и, следовательно, они являются коллоидными частицами, которые в воде образуют коллоидные растворы. Эти растворы характеризуются высокой вязкостью, способностью рассеивать лучи видимого света, не проходят сквозь полупроницаемые мембраны.
Вязкость раствора зависит от молекулярной массы и концентрации растворенного вещества. Чем выше молекулярная масса, тем раствор более вязкий. Белки как высокомолекулярные соединения образуют вязкие растворы. Например, раствор яичного белка в воде.
Коллоидные частицы не проходят через полупроницаемые мембраны (целлофан, коллоидную пленку), так как их поры меньше коллоидных частиц. Непроницаемыми для белка являются все биологические мембраны. Это свойство белковых растворов широко используется в медицине и химии для очистки белковых препаратов от посторонних примесей. Такой процесс разделения называется диализом. Явление диализа лежит в основе действия аппарата "искусственная почка", который широко используется в медицине для лечения острой почечной недостаточности.
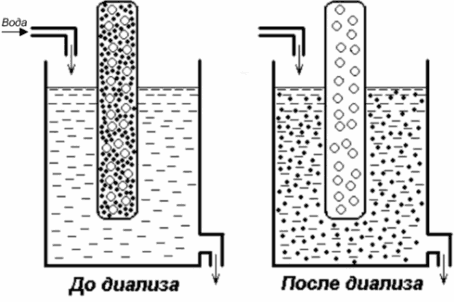
Диализ (белые крупные кружки - молекулы белка, черные - молекулы хлористого натрия)
