![]()
Первичная структура
Факторы, влияющие на образование вторичной структуры

Глава 4. Структура
4.1. Первичная структура
Представляет
собой линейную цепь аминокислот, расположенных в определенной
последовательности и соединенных между собой пептидными
связями. Пептидная связь образуется
за счет ![]() -карбоксильной
группы одной аминокислоты и
-карбоксильной
группы одной аминокислоты и ![]() -аминной
группы другой:
-аминной
группы другой:
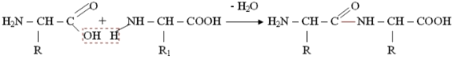
Пептидная связь вследствие
p, ![]() -сопряжения
-сопряжения
![]() -связи
карбонильной группы и р-орбитали атома N, на котором
находится не поделенная пара электронов, не может
рассматриваться как одинарная и вращение вокруг нее
практически отсутствует. По этой же причине хиральный
атом
-связи
карбонильной группы и р-орбитали атома N, на котором
находится не поделенная пара электронов, не может
рассматриваться как одинарная и вращение вокруг нее
практически отсутствует. По этой же причине хиральный
атом ![]() и карбонильный атом
и карбонильный атом ![]() любого i-го аминокислотного остатка пептидной цепи
и атомы N и
любого i-го аминокислотного остатка пептидной цепи
и атомы N и ![]() (i+1)-го
остатка находятся в одной плоскости. В этой же плоскости
находятся карбонильный атом О и амидный атом Н (однако
накопленный при изучении структуры белков материал
показывает, что это утверждение не совсем строго:
атомы, связанные с пептидным атомом азота,
находятся не в одной плоскости с ним, а образуют трехгранную
пирамиду с углами между связями, очень близкими к
120 градусам. Поэтому между плоскостями, образованными
атомами
(i+1)-го
остатка находятся в одной плоскости. В этой же плоскости
находятся карбонильный атом О и амидный атом Н (однако
накопленный при изучении структуры белков материал
показывает, что это утверждение не совсем строго:
атомы, связанные с пептидным атомом азота,
находятся не в одной плоскости с ним, а образуют трехгранную
пирамиду с углами между связями, очень близкими к
120 градусам. Поэтому между плоскостями, образованными
атомами ![]() ,
существует некоторый угол, отличающийся от 0. Но,
как правило, он не превышает 1 и не играет особой
роли). Поэтому геометрически полипептидную цепочку
можно рассматривать как образованную такими плоскими
фрагментами, содержащими каждый по шесть атомов. Взаимное
расположение этих фрагментов, как и всякое взаимное
расположение двух плоскостей, должно определятся двумя
углами. В качестве таковых принято брать торсионные
углы, характеризующие вращения вокруг
,
существует некоторый угол, отличающийся от 0. Но,
как правило, он не превышает 1 и не играет особой
роли). Поэтому геометрически полипептидную цепочку
можно рассматривать как образованную такими плоскими
фрагментами, содержащими каждый по шесть атомов. Взаимное
расположение этих фрагментов, как и всякое взаимное
расположение двух плоскостей, должно определятся двумя
углами. В качестве таковых принято брать торсионные
углы, характеризующие вращения вокруг ![]() -связей
N-
-связей
N-![]() и
и ![]() -
-![]() .
.
Геометрия любой молекулы определяется тремя группами геометрических характеристик ее химических связей - длинами связей, валентными углами и торсионными углами между связями, примыкающими к соседним атомам. Первые две группы в решающей мере определяются природой участвующих атомов и образующихся связей. Поэтому пространственная структура полимеров в основном определяется торсионными углами между звеньями полимерного остова молекул, т.е. конформацией полимерной цепи. Торсионный угол, т.е. угол поворота связи А-В вокруг связи В-С относительно связи С-D, определяется как угол между плоскостями, содержащими атомы А, В, С и атомы B, C, D.

В такой системе возможен случай, когда связи А-В и С-D расположены параллельно и находятся по одну сторону от связи В-С. Если рассматривать эту систему вдоль связи В-С, то связь А-В как бы заслоняет связь C-D, поэтому такая конформация называется заслоненной. Согласно рекомендациям международных союзов химии IUPAC (International Union of Pure and Applied Chemistry) и IUB (Inter-national Union of Biochemistry), угол между плоскостями ABC и BCD считается положительным, если для приведения конформации в заслоненное состояние путем поворота на угол не выше 180 ближнюю к наблюдателю связь нужно поворачивать по часовой стрелке. Если эту связь для получения заслоненной конформации нужно поворачивать против часовой стрелки, то угол считается отрицательным. Можно заметить, что это определение не зависит от того, какая из связей находится ближе к наблюдателю.
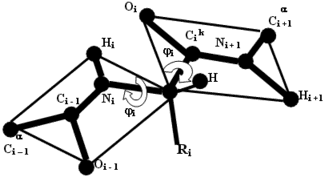
При
этом, как видно из рисунка, ориентация фрагмента,
содержащего атомы ![]() i+1
и
i+1
и ![]() i
[(i-1)-й фрагмент], и фрагмента, содержащего атомы
i
[(i-1)-й фрагмент], и фрагмента, содержащего атомы
![]() i
и
i
и ![]() i+1
(i-й фрагмент), определяется торсионными углами, соответствующими
вращению вокруг связи Ni-
i+1
(i-й фрагмент), определяется торсионными углами, соответствующими
вращению вокруг связи Ni-![]() i
и связи
i
и связи ![]() i-
i-![]() i.
Эти углы принято обозначать как
i.
Эти углы принято обозначать как ![]() и
и ![]() ,
в приведенном случае соответственно
,
в приведенном случае соответственно ![]() i
и
i
и ![]() i.
Их значениями для всех мономерных звеньев полипептидной
цепи в основном определяется геометрия этой цепи.
Никаких однозначных величин ни для значения каждого
из этих углов, ни для их комбинаций не существует,
хотя на те и на другие накладываются ограничения,
определяемые как свойствами самих пептидных фрагментов,
так и природой боковых радикалов, т.е. природой аминокислотных
остатков.
i.
Их значениями для всех мономерных звеньев полипептидной
цепи в основном определяется геометрия этой цепи.
Никаких однозначных величин ни для значения каждого
из этих углов, ни для их комбинаций не существует,
хотя на те и на другие накладываются ограничения,
определяемые как свойствами самих пептидных фрагментов,
так и природой боковых радикалов, т.е. природой аминокислотных
остатков.
К настоящему времени установлены последовательности аминокислот для нескольких тысяч различных белков. Запись структуры белков в виде развернутых структурных формул громоздка и не наглядна. Поэтому используется сокращенная форма записи - трехбуквенная или однобуквенная (молекула вазопрессина):

При
записи аминокислотной последовательности в полипептидных
или олигопептидных цепях с помощью сокращенной символики
предполагается, если это особо не оговорено, что ![]() -аминогруппа
находится слева, а
-аминогруппа
находится слева, а ![]() -карбоксильная
группа - справа. Соответствующие участки полипептидной
цепи называют N-концом (аминным концом) и С-концом
(карбоксильным концом), а аминокислотные остатки -
соответственно N-концевым и С-концевым остатками.
-карбоксильная
группа - справа. Соответствующие участки полипептидной
цепи называют N-концом (аминным концом) и С-концом
(карбоксильным концом), а аминокислотные остатки -
соответственно N-концевым и С-концевым остатками.
